Stoffwechsel im Allgemeinen
Im menschlichen Körper laufen die Stoffwechselwege über ein komplexes Netz enzymatischer Reaktionen, welche jeweils spezifische Produkte erbringen. Zunächst läßt
sich der Stoffwechsel aber in zwei große Bereiche aufteilen. Es gibt aufbauende Wege (Anabolismus) und abbauende Wege (Katabolismus). Das bedeutet, der Anabolismus katalysiert endergonische,
aufbauende Reaktionen, welche zu komplexeren Stoffwechselprodukten führen, während der Katabolismus exergonisch wirkt und einfachere, kleinere Produkte hervorbringt.
Zu beachten
ist hierbei, dass viele katabolische Reaktionen auf ein Zwischenprodukt zu arbeiten. Dieses kann dann einen einheitlichen Weg des Stoffwechsels einschlagen.
Auf diesem Weg kann man die
genetische Codierung von Stoffwechselwegen verkürzen, wie auch einen einheitlichen Regulationsmechanismus schaffen.
Diese wenigen Stoffwechselzwischenprodukte dienen dann auch wieder dem Aufbau vieler Produkte des Anabolismus.
Ganz allgemein gibt es vier Hauptcharakteristika des Stoffwechsels, die man behalten sollte:
- Stoffwechselwege sind irreversibel. Abbauende Wege laufen so stark exergonisch ab, so dass der Körper diese Energie für einen möglichen Rückweg mit dem gleichen
Reaktionsmechanismus nicht aufbringen kann. Aus diesem Grund existieren immer nur andere Mechanismen als Rückreaktion.
- Jede Stoffwechselkette hat einen ersten, bestimmenden Schritt.
Ist dieser Initialschritt vollzogen, folgen in der Regel die weiteren Schritte gemäß dem Reaktionsgleichgewicht.
- Stoffwechselwege werden in der Regel in der ersten Reaktion reguliert.
Läuft also ein Weg über sehr viele Reaktionen ab, kann man davon ausgehen, dass der schrittgebende
Mechanismus an einer der ersten Reaktionen wirkt bzw. reguliert.
- Die Orte der Stoffwechselprozesse sind im eukaryontischen Körper festgelegt. Damit ist gemeint, dass es bestimmte
Orte gibt, an denen bestimmte Reaktionen stattfinden. An anderen Orten werden aber oftmals die Produkte dieser Reaktionen benötigt. Aus diesem Grund hat sich die Natur Transportmittel
ausgedacht, welche Metabolite von einem Ort zu einem anderen befördern.
Relevante Stoffwechselwege
Da das komplette Wissen aller Stoffwechselvorgänge einer Zelle zu viel für die Vorbereitung auf eine Biochemieklausur der Vorklinik darstellt, lassen sich die wichtigen Vorgänge
wie folgt reduzieren:
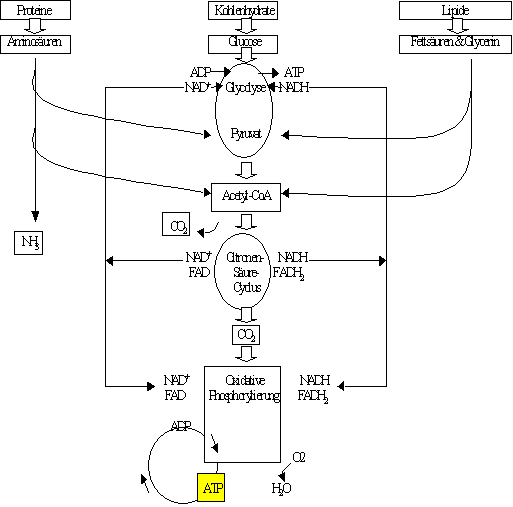

Phosphatverbindungen
Wie die vorige Zeichnung zeigte, enden die wichtigsten katabolischen Wege des Stoffwechsels in der Oxidativen Phosphorylierung. Es wird ATP aus ADP gebildet. Nun fragt man sich aber, wieso
wird ATP gerade gebildet, und wieso ist es ein so energiereicher Stoff?
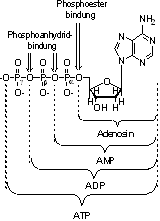
Kümmern wir uns zunächst um den Aufbau des ATPs. ATP ist eine Abkürzung für Adenosin-Tri-Phosphat, also handelt es sich um das Nucleosid Adenosin und drei Phosphatreste.
Der erste Rest ist an das Nucleotid mittels einer Phosphoesterbindung gebunden, die beiden anderen durch eine Phosphoanhydridbindung.
Phosphorylgruppenübertragung
Diese Reaktionen sind für den Organismus von überragender Bedeutung, da währenddessen genug Energie frei
Der Reaktionsablauf allgemein hat die Formel:
wird, um sonst zu endergonische Prozesse antreiben zu können.
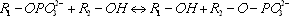
Die wichtigsten Reaktionen dieser Art sind die von ATP:
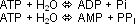
Pi ist die Abkürzung für Orthophosphat, PPi die Abkürzung für Pyrophosphat.
Die Regeneration des ATP erfolgt umgekehrt über noch stärker exergonische Stoffwechselprozesse.
Der Nutzen solcher Phosphorylgruppenübertragungen besteht darin, dass man damit einem Molekül eine große Menge freier Enthalpie für weitere Reaktionen verschafft,
während diese Gruppen jedoch relativ stabil gegenüber einer Hydrolyse sind.
Energiereiche Verbindungen
- Bindungen, deren hydrolytische Spaltung stark exergonisch ist
- nicht verwechseln mit der sog. Bindungsenergie
- energiereiche Bindung mittels einer Schlangenlinie gekennzeichnet
› z.B. beim ATP: AR-P~P~P.
- beim ATP sind die beiden letzten Phosphorylgruppen sehr “energiereich” gebunden
- Grund liegt in der Resonanzstabilisierung:
› starke elektronenziehende Kräfte in den Anhydridbindungen
› ausgehend von den Phosphorylgruppen, die auf den Brückensauerstoff wirken
› bei der Hydrolyse der Bindung verschwindet diese Konkurrenz
› außerdem stoßen sich die geladenen Gruppen der Phosphoanhydride gegenseitig ab
› weitere Spannung auf die Bindung
- wichtigen Vorteil des ATP gegenüber Verbindungen mit anderen Säureanhydriden:
› Phosphoanhydridbindungen benötigen bei einer normalen Hydrolyse eine hohe Aktivierungsenergie
› bei enzymatischer Hydrolyse minimiert
› ATP unter physiologischen Bedingungen sehr stabil
› in enzymatischen Reaktionen aber ein schneller Energielieferant
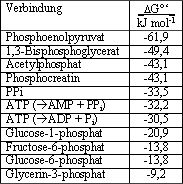
Neben ATP existieren im Organismus weitere energiereiche Verbindungen:
Wie man erkennt, ist die freie Enthalpie wesentlich größer als die von ATP.
› es kommen weitere, destabilisierende Merkmale zur Wirkung
Säureanhydride
Phosphorsäureanhydride
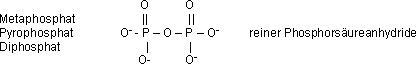
unreine Phosphorsäureanhydride:

Thioester 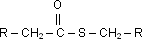
Phosphoenolester
Phosphorester sind i. d. R. nicht energiereich
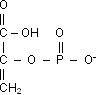
P | N – Bindungen

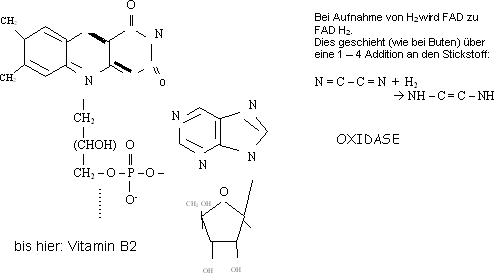
FAD (Flavin Adenin Dinucleotid)
(nützlich zum AS Abbau mit Desaminierung)
NAD (Niacinsäureamid Adenin Dinucleotid)
(arbeitet intramitochondrial) Nicotinsäure (mit OH)
mit NH2 Nicotinsäureamid, Niacinamid (spez. für B – Vitamine) 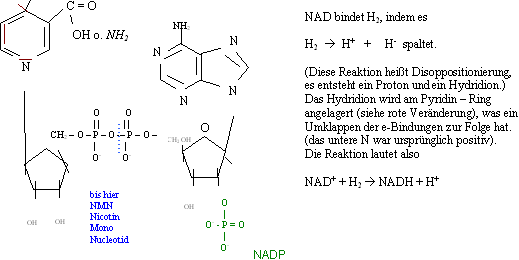
Die Rolle des ATP
- ATP fungiert mit seinem mittelgroßen Übertragungspotential als Vermittler
› zwischen sehr energiereichen Phosphoryldonoren und energieärmeren Phosphorylakzeptoren.
- Übertragung des Phosphorylrestes auf und von ATP übernimmt Enzymklasse der Kinasen
› in der Regel wenig substratspezifisch
- stark exergone Gruppenübertragungen werden für endergone Reaktionen genutzt
› beide Reaktionen über ein Enzym gekoppelt
Bildung von ATP
- Substratkettenphosphorylierung:
- Phosphorylgruppe von einer energiereicheren Verbindung auf ADP übertragen
- Oxidative Phosphorylierung:
- oxidativer Stoffwechsel bewirkt den Aufbau eines Protonengradienten über eine Membran
- bei Ausgleich dieses Gradienten durch die Membran wird Energie frei
› wird gespeichert in Bindung von Pi an ADP.
- Adenylylkinase-Reaktion:
- in machen Reaktionen statt ADP AMP gebildet
- Zwischenreaktion bei ATP-Mangel:
› Adenylylkinase-Reaktion 2 ADP ‹› AMP + ATP
› katalysierendes Enzym: Adenylylkinase
Verbrauch des ATP
ATP wird in seiner Funktion als universeller Energieträger auf verschiedene Weise verbraucht:
- Im frühen Stadium des Nährstoffabbaus:
- erste Abschnitte der Glycolyse: ATP wird gespalten
› Phosphorylierung von Glucose-6-phosphat und Fructose-1,6-bisphosphat
- Umwandlung verschiedener Nucleosidtriphosphate:
- weitere Verbindungen von Nucleosidtriphosphaten (NTP), wie CTP, GTP, UTP
- in manchen Stoffwechselprozessen statt ATP verwendet
- praktisch gleiche freie Standardenthalpie
- Physiologische Prozesse:
- Muskelkontraktion, Ionenpumpen (!)
- Zusätzliche Spaltung:
- stark endergonische Prozesse benötigen mehr Energie, als die Hydrolyse von ATP zu ADP + Pi bietet
› ATP zu AMP + PPi gespalten; liefert etwa die gleiche Energie
- zusätzlich PPi zu zwei Molekülen Pi durch das Enzym
Anorganische Pyrophosphatase gespalten
› nochmals ungefähr die gleiche Energie frei (Beispiel: Fettsäureoxidation)
Kontrolle der ATP-Produktion
Die Produktion von ATP bedarf einer spezifischen Kontrolle, da der Körper immer nur so viel ATP produzieren sollte, wie er im Augenblick auch braucht. Zum Beispiel ist der ATP Verbrauch
während des Schlafes wesentlich geringer als im Wachzustand, wiederum bis zu 100mal höher bei anstrengender Betätigung. Die Regulation der ATP Synthese wird hauptsächlich über
die katabolischen Wege der Kohlenhydrate vorgenommen. Allerdings gibt es neben einem direkten Einfluß durch Adenosinnucleotide auch Einflüsse durch die NADH/NAD+ Konzentration,
die sich auf die Elektronentransportkette ausübt. Auch der Citrat-Cyclus erhält eine Kontrolle über die Geschwindigkeit der Glycolyse durch eine direkte Hemmung der PFK durch
Citrat. Der Gesamtzusammenhang sei hier in einer Grafik dargestellt.
Die Physiologische Bedeutung aeroben und anaeroben Stoffwechsels
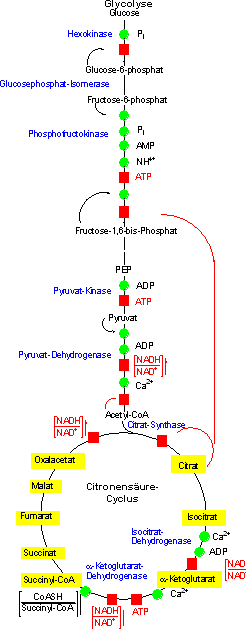 Die aerobe ATP Produktion hat gegenüber der anaeroben deutliche Vorteile. Der zunächst wohl deutlichste ist die wesentlich höhere Effektivität. Während bei der Lactat
Fermentation nur zwei ATP pro Molekül Glucose abfallen, sind dies beim aeroben Stoffwechsel 38 Moleküle ATP: Die aerobe ATP Produktion hat gegenüber der anaeroben deutliche Vorteile. Der zunächst wohl deutlichste ist die wesentlich höhere Effektivität. Während bei der Lactat
Fermentation nur zwei ATP pro Molekül Glucose abfallen, sind dies beim aeroben Stoffwechsel 38 Moleküle ATP:
Anaerobe Glycolyse:
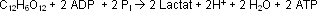
Aerober Glucosestoffwechsel:
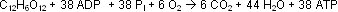
Allerdings hat der anaerobe Stoffwechsel auch wichtige Vorteile. Durch seine kurzen Abbaumechanismen und die Tatsache,
dass er ohne Sauerstoff auskommt ist er wichtig in Gewebe, das
spontan an Änderungen des Verbrauchs reagieren müssen, wie z.B. Muskelgewebe. Leider existiert dabei auch ein gewichtiges Problem. Das angehäufte Lactat senkt den PH Spiegel
der Zelle. Außerdem wird ebenfalls nach relativ kurzer Zeit das ATP verbraucht, da der Ertrag der gespeicherten Glucose bzw. des Glycogens sehr niedrig ist. Ist irgendwann der ATP Gewinn
erschöpft, können die Ionenpumpen, die einen Sollwert der Ionenkonzentration aufrechterhalten, nicht mehr arbeiten. Das aber führt zu einem Einstrom von Flüssigkeit. Die
Zelle bläht sich auf und ihre Membran wird permeabel. Außerdem können nun Lysozyme, die bei niedrigem PH-Wert arbeiten, die Zelle zersetzen. |
