Die Purin- und Pyrimidinbasen der Nukleinsäuren
Bei den Grundstrukturen der Purine und Pyrimidine sind die unterschiedlichen Nummerie-rungen der Ringe zu beachten!
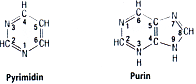
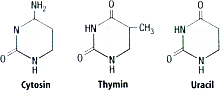
Die Pyrimidinbasen:
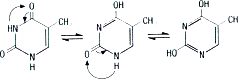
Oxypurine und Oxypyrimidine, d.h. Purine bzw. Pyrimidine mit einer O-Rest, zeigen das Phänomen der Keto-Enol-Tautomerie.
Zur korrekten Informationsübertagung bei der Trans-kription in der
Zelle muss allerdings die Ketoform vorliegen. Diese wird im Gleichgewicht auch stark bevorzugt wird.
Keto-Enol-Tautomerie von
Oxypurinen und Oxypyrimidinen

Der Aufbau von Nucleosiden und Nucleotiden
Nukleotide sind die Bausteine der Nukleinsäuren, sprich der DNA und der RNA.
Nucleosid = Base + Ribose (Zucker)
Nucleotid = Base + Ribose + 1-3 Phosporsäuregruppe(n)
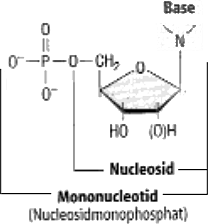
Mononucleotid = Nucleosidmonophospat (NMP) Base + Ribose + 1 Phosphorsäuregruppe
Dinucleotid = Nucleosiddiphosphat (NDP) Base + Ribose + 2 Phosphorsäuregruppen
Trinucleotid = Nucleosidtriphosphat (NTP) Base + Ribose + 3 Phosphorsäuregruppen
Einige Beispiele:
Base: |
Nucleosid: |
Nucleosidmonophosphat: |
Adenin (A)
Guanin (G)
Thymin (T)
Cytosin (C)
Hypoxanthin |
Adenosin
Guanosin
Thymidin
Cytididn
Inosin |
Adenosinmp = AMP
Guanosinmp = GMP
Thymidinmp = TMP
Cytidinmp = CMP
Inosinmp = IMP |
Die Basen werden über eine N-glykosidische Bindung an das C 1’-Atom der Ribose (RNA) bzw. der Desoxyribose (DNA) gehängt. Die Phosphorsäuregruppen werden am C 5’–Atom
des Zuckers befestigt. In einem Polynucleotid kommen nie Ribose und Desoxyribose neben-einander vor!
DNA und RNA unterscheiden sich sehr stark in ihren Zerfallsgeschwindigkeiten. Während die RNA in Wasser eine Halbwertszeit von Stunden hat, verfügt die DNA über eine Halbwertszeit von
Jahrtausenden!
Beispiele eines RNA- Mononucleotides und eines DNA- Mononucleotides:
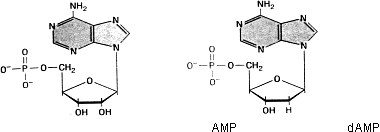
Bedeutung der Nucleotiden:
- Extrazelluläre Signalmoleküle, z.B. Durchblutungsregulierung vieler Gewebe durch Adenosin
- Überträger von Methylgruppen (Bsp. S-Adenosylmethionin (SAM) = aktives Methio-nin)
- Veränderte Nucleoside werden bei Tumorbekämpfung und Viruserkrankungen eingesetzt (s. später)
Ein weiteres sehr wichtiges Signalmolekül ist das cyclische AMP, kurz cAMP.
Mononucleotide sind Träger energiereicher Phosphatgruppen, die eine Anlagerung weiterer Phosphatgruppen begünstigen. In Zellen werden laufend Phosphatgruppen und somit Energie vom einem Nucleosidtriphosphat
auf ein Nucleosiddiphosphat übertragen .
Beispiele für Übertragung von g-Phosphatresten (3. Phosphatgruppe bei TP):
UDP + ATP ‹› UTP + ADP
IDP + ATP ‹› ITP + ADP
GDP + ATP ‹› GTP + ADP
3. Biosynthese von Purinnucleotiden
Der Purinkern wird aus den AS Gln, Asp, Gly sowie Formiat und HCO3- aufgebaut:
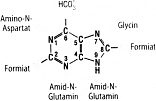
Die Biosynthese erfolgt zuerst über die offene Form des Ribonucleotides, die später geschlos-sen wird. Die Synthese des IMP liegt allen anderen Purinnucleotiden zugrunde:
- Ribose-5-Phosphat reagiert mit ATP unter Abspaltung vom AMP zu 5-Phosphoribosyl-1-Pyrophosphat (PRPP). Benötigtes Enzym: Ribosephosphat-Pyro-phosphokinase.
- Unter Katalyse durch PRPP-Amidotransferase
reagiert PRPP mit Glutamin unter Abspaltung von Pyrophosphat und Glutamat zu 5-Phosporibosylamin.
- In 9 Schritten wird das C- und N-Skelett des Purins synthetisiert. Es entsteht dabei das Inosinmonophosphat
aus dem die weiteren MP gebildet werden können.
Biosynthese von Pyrimidinnucleotide
Aspartat und Carbamylphosphat liefern die C- und die N-Atome für den Pyrimidinkern. Carbamylphosphat wird auch für die Harnstoffsynthese verwendet.
Wie schon das IMP bei der Purinsynthese ist das UMP der Grundbaustein für alle weiteren MP in der Pyrimidinsynthese.
Aus UMP wird durch zweimalige Anlagerung von Phosphatgruppen (aus ATP) UTP hergestellt. Um CTP zu synthetisieren werden Glutamin und ATP benötigt, die zu Glutamat, ADP und anorganischem Phosphat
reagieren.
Auch in der Pyrimidinsynthese finden wir multifunktionelle Enzymproteine: Es sind deren 3 für insgesamt 6 Biosyntheseschritte. Multifunktionelle Proteine enthalten mehrere aktive Domänen,
also mehrere katalytisch aktive Zentren.
- CAD-Protein: enthält Aspartattranscarbamylase, Carbamylphosphatase, Dihydrooro-tase
- Enzym mit Orotatphosphoribosyltransferase und OMP- Decarboxylase
- Dihydroorotat- Dehydrogenase. Nur 1 Funktion
Biosynthese von Desoxyribonucleotiden
Der entscheidende Schritt ist die Umwandlung von Ribonucleotiden in Desoxyribonucleotide. Das verantwortliche Enzym heisst: Ribonucleotid-Reduktase
Reaktionsgleichung:
Ribonucleotiddiphosphat + NADPH + H+ › Desoxyribonucleotiddiphosphat + NADP+ + H2O
Herkunft des H+ für die Biosynthese: [H] wird von einem Molekül auf das nächste übertragen!
Desoxyribonucletoiddiphosphat (dNDP) + ATP ‹› dNTP + ADP
Die Ribonucletotidreduktase wird durch ATP aktiviert und durch dATP inhibiert.
Thymidinnucleotide entstehen durch Methylierung von dUMP. Das verantwortliche Enzym heisst Thymidylat-Synthase:
dUMP + N5, N10- Methylen-Tetrahydroflat › dTMP + 7,8- Dihydrofolat
Hemmstoffe der Purin- und Pyrimidinsynthese
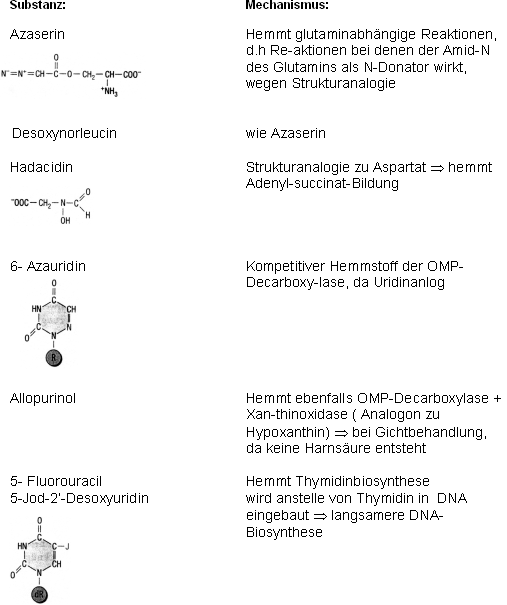
Aminopterin/ Amethopterin = Methotrexat Analoge der Folsäure › hemmen die Di-hydrofolatreduktase› keine Neusynthese von Thymidinnucleotiden
Medizinischer Hinweis: Methotrexat ist Zystostatika in der Tumortherapie.
Regulation der Biosynthese von Purin- und Pyrimidinnucleotiden
Die Purinbiosynthese wird v.a. auf der Stufe der PRPP-Amidotransferase reguliert. Es exis-tieren eine aktive, monomere Form und eine inaktive, dimere Form.
PRPP stimuliert den Übergang von der dimeren Form (zweiteilig) in die monomere Form Þ aktiviert die PRPP-Amidotransferase und somit die IMP-Biosynthese.
Alle Purinnucleotide (Endprodukte) bewirken eine Verschiebung des Gleichgewichtes auf die dimere Seite oder anders gesagt eine Inhibition des Enzyms.
Eine weitere Regulationsmöglichkeit besteht in der „Cross-Regulation“ bei der Umwandlung von IMP in AMP/ADP/ATP bzw. GMP/GDP/GTP.
Das CAD-Protein Dihydroorotatdehydrogenase reguliert die Pyrimidinbiosynthese.
Allosterisch reguliertes Enzym: Carbamylophospatsynthetase II Þ wird durch das Endpro-dukt der Biosynthese , UTP, gehemmt (allosterisch = nicht im aktiven Zentrum des Enzyms)
PRPP ist ein wirksamer allosterischer Aktivator
Dihydroorotase und Dihydroorotatdehydrogenase Aktivität wird durch Orotat (Produkt der Biosynthese) gehemmt.
Wiederverwertung von Purinen und Pyrimidinen
Während beim intrazellulärem Abbau von Nucleinsäuren Purine und Pyrimidine entstehen, entstehen bei der intestinalen Resorption von Nahrungsstoffen die Purin- und Pyriminbasen.
Für die Recyclierung von Adenin, Hypoxanthin und Guanin werden zwei Enzyme benötigt:
- Adenin-Phosphoribosyltransferase (APRT): Adenin ------PRPP abhängig----› AMP
Enzym wird durch Adenosinnucleotide (bes. AMP) gehemmt
- Hypoxanthin-Guanin-Phosphoribosyltransferase (HGPRT): Recycling von Hypoxan-thin und Guanin. PRPP ist hier Phosphoribosyldonator. Hemmung
erfolgt durch die Endprodukte IMP und GMP.
Da ein System von mehr als 15 Enzymen Purine, Purinnucleoside und Purinnucleotide inei-nander überführt, ist der Organismus zu einem gewissen Grad unabhängig von der Biosyn-these aus
den Grundbausteinen.
Wichtige Bestandteile des Recyclingsystemes
Purinnucleotidcyclus
IMP Adenylosuccinat-Synthetase › Adenylosuccinat ›Adenylosuccinat-Lyase › AMP › AMP-Desaminase › IMP
Bei gesteigerter Muskelarbeit stiegt die NH3 Produktion im Muskel. Eine Störung des Purinnucleotidcyclus bewirkt also eine Störung der Muskeltätigkeit!
Die Transformation von Aspartat in Fumarat ist für den Citrat-Cyclus wichtig Þ Bestückung des Citrat-Cyclus mit anaplerotischen Reaktionen (den Cyclus auffüllend), d.h. Versorgung
mit Cycluszwischenprodukten die bei der Biosynthese wieder abfliessen.
Pyrimidinnucleotidcyclus:
- Biosynthese von 400-700 mg pro Tag ( Purine ebenfalls soviel)
- Recyclingsystem: vorhanden, aber wenig bekannt
- Grösster Bedarf wird durch Recycling gedeckt
ZNS: schlechte Enzymausstattung für Pyrimidinbiosynthese, dafür höchste Recycling-aktivität!
Auch Erythrocyten weisen eine grosse Menge an Recyclingenzymen auf. Sie besitzen ja keinen Kern für Syntheseaktivitäten.
Abbau von Purinnucleotiden
Harnsäure: Endprodukt bei Primaten, Vögeln, einigen Reptilien
Schwer wasserlöslich
4-6 mmol/tag scheidet der Mensch aus. Das entspricht der Biosynthesemenge.
Allantoin: weiteres Abbauprodukt der Harnsäure, andere Säuger, Reptilien, Mollusken
Besser wasserlöslich als Harnsäure
Fische: Spalten Allantoin in Harnstoff und Glyoxylsäure
Beim Purinabbau wird keine Energie gewonnen!
Abbau von Pyrimidinnucleotiden
Der Pyrimidinabbau erfolgt in der Leber. Dabei wird Energie frei, da Acetat und Propionat oxidierbare Verbindungen sind.
Pathobiochemie – Purinstoffwechsel
Die Hemmung der Purinnucleotidbiosynthese, d.h. Blockierung der Nucleinsäuren-Biosyn-these, durch Metabolitanaloge hat Zelltod zur Folge.
Bei einer Überproduktion von Purinnucleotiden steigt die Abbaumenge und Harnsäure lagert sich an: Hyperuricämie. Es kann nur eine bestimmte Menge Harnsäure gebunden und ausgeschieden
werden.
Man unterscheidet zwischen primärer und sekundärer Hyperuricämie. Die primäre ist erblich bedingt und bei ihr sind die Biosynthese und/oder die Ausscheidung betroffen . Die sekundäre
ist eine Folge erhöhten Purinbasenabbaus durch Zelltod ( z.B. wegen Krankheit) oder wegen einer Nierenerkrankung die die Ausscheidung behindert.
Gicht: Harnsäureablagerung in Gelenken, Schleimbeuteln, Sehnenscheiden, Subcutis, Nieren-mark. Ist von chronischen Krankheiten und akuten Entzündungsschüben begleitet.
Bei Luxuskonsum, d.h. hoher Fleischkonsum, werden dem Körper viele Purinbasen zuge-führt, was wiederum erhöhte Harnsäuremengen zur Folge hat. |
