Für Chemiker ist es zweckmässig, die organischen Verbindungen in zwei grosse Klassen einzuteilen, in aliphatische und aromatische Verbindungen. Die Bezeichnungen aliphatisch (fettartig)
und aromatisch (wohlriechend) haben allerdings ihre ursprüngliche Bedeutung eigebüsst. Zu den Aliphaten zählen alle Verbindungen, die wir bisher besprochen haben: Alkane, Cycloalkane,
Alkene, Cycloalkene. Aromaten sind das Bezol und ihm verwandte Verbindungen.
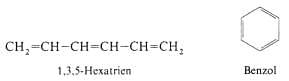
Alle 6 C-Atome des Benzols sind sp2-hybridisiert und liegen in einer Ebene. Als Folge der Delokalisierung der p-Elektronen gibt es im Benzol keine Doppel- und Einfachbindungen mehr. Der Sechsring ist
symmetrisch und alle C-C-Bindungen gleich lang (0.139 nm) und damit kürzer als C-C-Einfachbindungen. (0.154nm) und länger als normale C=C-Doppelbindungen (0.133nm)
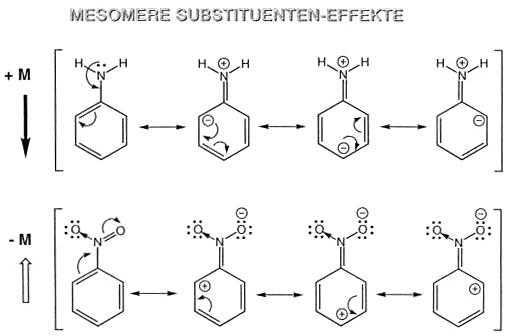
Man hat für Systeme mit delokalisierten p-Elektronen den Begriff Mesomerie bzw. Resonanz geprägt und bezeichnete die Formeln, die dies ausdrücken sollen, als mesomere Grenzformeln (=
Resonanzstrukturen). Zur Mesomerie befähigte Systeme sind aufgrund von Besonderheiten ihrer Molekülorbitale energieärmer als Verbindungen, bei denen dies nicht möglich ist. Aromaten
nehmen durch die cyclische Konjugation dabei eine Sonderstellung ein. Der Energiebetrag, der das Benzol vom offenkettigen Trien unterscheidet heisst Mesomerieenergie (= Resonanzenergie) und macht
etwa 125 kJ/mol aus.
Reaktionen des Benzols
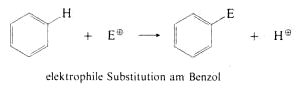
Die typische Reaktion der Aromaten ist die Substitution. Ein H-Atom wird direkt durch ein anderes Atom oder einen Rest ersetzt. Der aromatische Charakter des Rings bleibt erhalten Das angreifende Reagens
ist ein Elektrophil (E+), aus dem Aromaten wird ein Proton (H+) abgespalten.
Befindet sich schon ein Substituent am Benzolring, dann gibt es für einen zweiten drei verschiedene Positionen, die als ortho (o), meta (m) und para (p) bezeichnet werden.
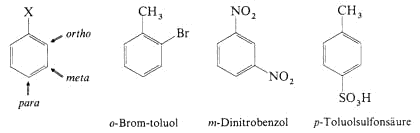
Bei mehr als zwei Substituenten am Ring werden die C-Atome von 1-6 numeriert und Zahlen vor die Substituenten gesetzt. Wird der Benzolring selbst als Substituent aufgefasst, bezeichnet man die C6H5-Einheit
als Phenyl bzw. aromatische Reste allgemein als Arylreste.
Mechanismus der elektrophilen aromatischen Substitution
Ein aromatisches System stellt, wie jede Doppelbindung, einen Ort hoher Elektronendichte dar.
1.Angriff des Elektrophils Br+ auf das p-System des Benzols und Ausbildung einer s-Bindung mit einem Ring-C-Atom
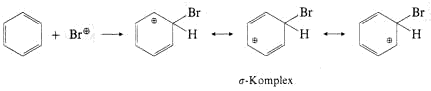
Regioselektivität der armoatischen Substitution
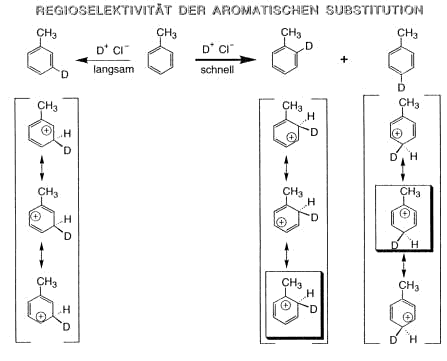
Ortho und para werden bevorzugt!
Begründung
Ein tertiäres Carbenium-Ion ist energetisch günstiger als ein sekundäres.
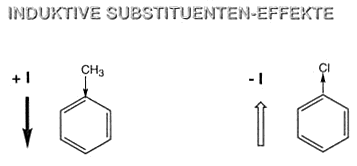
Als induktiver Effekt wird die Verschiebung der Bindungselektonen entlang der Achse einer s-Bindung bezeichnet. Der induktive Effekt ist in der verschiedenen EN der miteinander gebundenen Atome begründet.
Induktive Substituenten-Effekte

Regioselektivität der Additionsreaktion
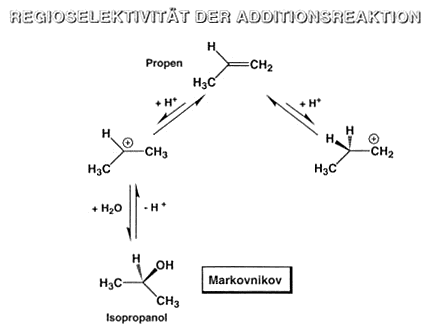
Begründung:
- ist energetisch ärmer als
- und wird deshalb bevorzugt
Oder: “Wer hat, dem wird gegeben“. CH2 hat schon 2 H und bekommt deshalb ein 3.H
Die C-H-Bindung ist nur wenig polarisierbar, da die Kerne sehr nahe beieinander liegen. Die C-C-Bindung ist leichter polarisierbar, weil die e- in der 2.Schale liegen.
Regel von Markovnikov:
Der elektrophile Teil des Reagens verbindet sich mit dem wasserstoffreicheren C-Atom der Doppelbindung.
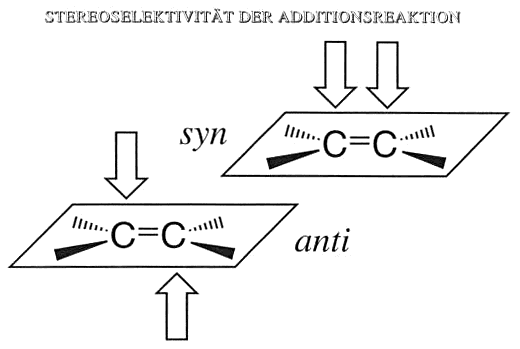
Stereoselektivität der Additionsreaktion
|
